Fat Man, a bomba atômica que foi detonada sobre Nagasaki em agosto de 1945.
As armas nucleares são explosivos com poder de destruição em massa, cuja força provém de reações que ocorrem nos núcleos dos átomos. Há dois tipos de reações nucleares: a fissão e a fusão nuclear, que liberam energia na forma de calor. Existem dois tipos principais de armas nucleares, as bombas de fissão (bombas atômicas) e as bombas de fusão (bombas de hidrogênio).
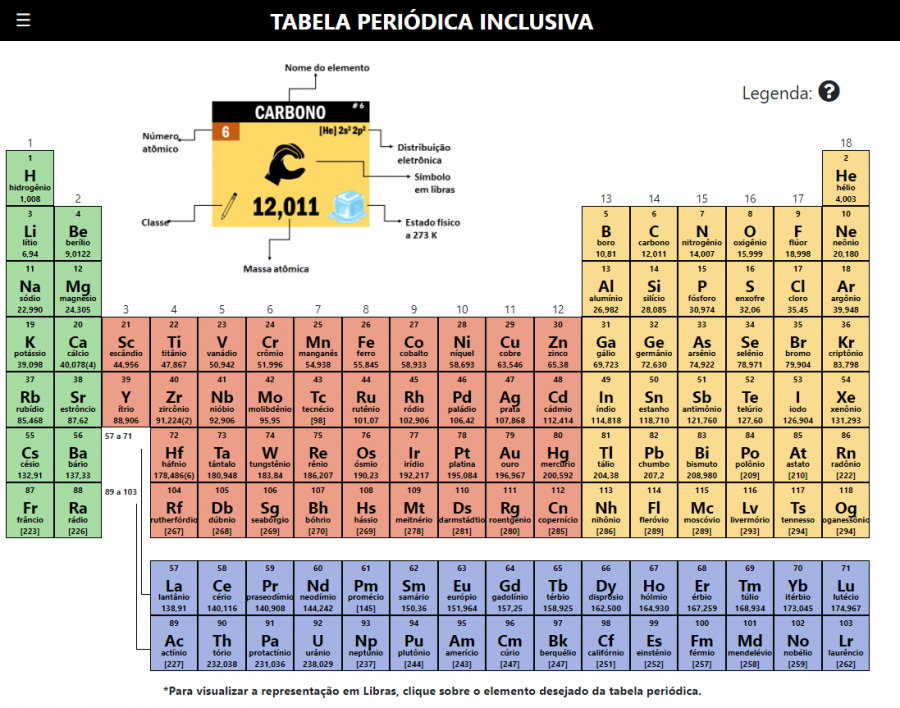
Nas bombas atômicas a energia explosiva é a fissão nuclear. Um átomo pesado e instável tem seu núcleo bombardeado por partículas em alta velocidade, rompendo-se em átomos menores, liberando energia.
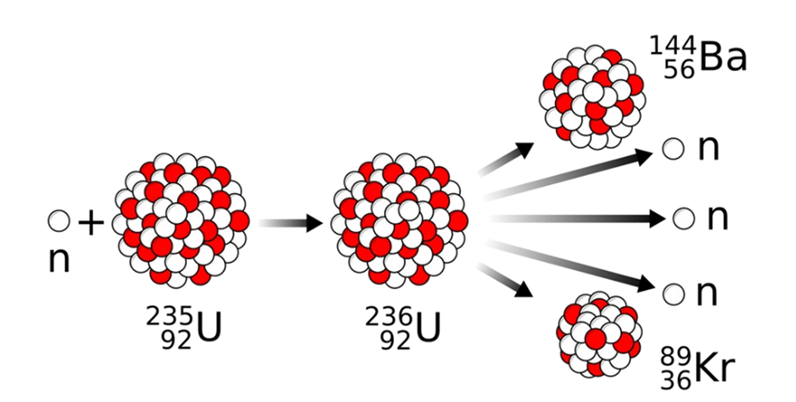
O urânio é o elemento mais comumente empregado na produção das bombas atômicas. O isótopo urânio-235(235U) é o mais utilizado. O bombardeamento do núcleo atômico do urânio-235 com um nêutron produz o isótopo físsil urânio-236 (236U), que sofre fissão nuclear gerando dois átomos menores, nêutrons e liberando uma quantidade enorme de energia na forma de calor. Cada nêutron liberado na fissão do urânio bombardeará outros átomos, promovendo uma reação em cadeia.
Processo de fissão nuclear do Urânio-235.
As primeiras explosões com bombas atômicas ocorreram em 1945, durante a Segunda Guerra Mundial. A bomba atômica Little Boy foi produzida pelos EUA através do projeto Manhattan e detonada na cidade de Hiroshima no Japão, em 6 de agosto de 1945. Sua base era de 65 quilos de urânio-235, produzindo energia equivalente à 15 mil toneladas de dinamite, provocando a morte instantânea de 70 mil pessoas e deixando um número equivalente de pessoas feridas. A detonação da bomba, produziu uma bola de fogo, que podia ser vista à 3 km de distância. A destruição causou um vento que varreu a cidade à 1500km/h em um raio de 2 km do centro da explosão. Como um sopro, a maioria das pessoas foi a óbito em poucas horas.
Bomba Little Boy antes de ser montada no Enola Gay.
Três dias após o primeiro ataque, ocorreu um segundo ataque, à cidade Nagasaki, que foi bombardeada pela Fat Man, bomba à base de plutônio-239, sendo 50% mais poderosa que a Little Boy. Apesar de seu maior potencial de destruição, a detonação da Fat Man levou à morte imediata de 40 mil pessoas, em decorrência das características da cidade, que se encontrava entre montanhas, fazendo com que fosse protegida por sua forma geográfica. Em função da alta radiação no local, muitos sobreviventes morreram nos dias seguintes.
Einstein e as armas nucleares
O físico alemão Albert Einstein tem sua imagem associada às armas nucleares, porque o desenvolvimento da bomba atômica só foi possível após a compreensão da relação entre massa e energia, através da fórmula E=m.c2, proposta por ele. Ao que tudo indica, a participação de Einstein no processo de criação da bomba atômica foi mais além da teoria. Em 1939, Einstein redigiu e enviou uma carta ao presidente dos EUA, Franklin Roosevelt, alertando-o para que os EUA começassem a produzir a bomba atômica, antes que os nazistas criassem suas próprias armas.
A partir da carta, o presidente americano deu início ao projeto Manhattan, que desenvolveu as primeiras armas nucleares, inclusive as bombas Little Boy e Fat Man. Apesar de sua contribuição indireta, Einstein era considerado um pacifista, não tendo participado diretamente do projeto.
A fim de evitar futuros ataques, em 1968, foi criado o tratado de não proliferação de armas nucleares, que entrou em vigor internacionalmente em 1970, após a assinatura de 189 países. O tratado conta com leis bem especificas sobre a proibição do uso de armas nucleares, deixando apenas para fins pacíficos o uso da energia nuclear. Já em 2017, foi proposto o Tratado de Proibição das Armas Nucleares, que até o ano de 2021 foi assinado por 122 países.
Por Ana Flávia Silveira Santos, Natalia Lopes de Araújo, Nathália Geovana Calejon Gomes, Pedro William Maia e Alda Ernestina.
Artigo publicado na Revista IFMG Com Ciência